The-Periodic-Table-Of-Oxidation-States-2016.png
0.30MB
산화수는 하나의 물질(분자, 이온 화합물, 홑원소 물질 등) 내에서 전자의 교환이 완전히 일어났다고 가정하였을 때 물질을 이루는 특정 원자가 갖게 되는 전하수를 말하며 산화 상태라고도 한다.
어떤 물질에서 원소의 산화정도를 나타내는 가상적인 전하량이므로 반드시 이온전하를 의미하지는 않는다.
보통 복잡한 반응에서 산화와 환원을 판단할 때 유용하게 사용된다.
원자에서 화학 변화를 통해 산화수의 증가가 이루어질 경우에는 산화라고 칭하며, 그 반대로 산화수가 감소될 경우에는 환원이라고 이야기 한다.
즉 반응물과 생성물을 이루는 원소들이 반응 후 산화수가 증가하면 그 원소는 산화된 것이며, 산화수가 반응 후 감소하면 그 원소는 환원된 것이다. 형식적으로 전하가 끌려갔다는 것을 표현한다.
이온 결합에서는 전자의 이동이 분명하지만 공유 결합에서는 그렇지 않으므로, 공유 결합에서는 전기 음성도가 큰 원자가 공유 전자쌍을 완전히 차지한다고 가정하고 산화수를 구한다.
계산법은 고등학교 화학 교재를 참고하자.
아래는 원소가 가질 수 있는 산화수를 주기율표에 나타낸 그림이다.
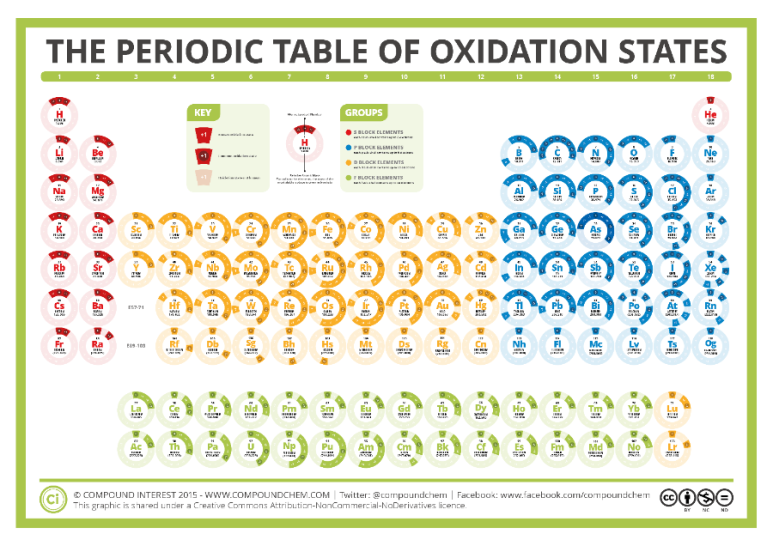
다운 받은 파일을 확대해서 보면, 원 둘레에 나타낸 숫자가 가능한 산화수이며, 진한 동그라미로 표시된 숫자는 그 원소가 주로 갖는 산화수이다.
'화학' 카테고리의 다른 글
| [사고력확장] 산화철의 종류 + 시아노박테리아 + 호상철광층 (0) | 2025.04.22 |
|---|---|
| 기체의 용해도 gas solubility (0) | 2025.03.25 |
| anode가 양극이야 음극이야? (0) | 2025.01.05 |
| 금속의 이온화 경향 (1) | 2024.12.08 |